Diagnostic potential of cryptic exon-derived peptides in serum extracellular vesicles for sporadic amyotrophic lateral sclerosis
筋萎縮性側索硬化症(amyotrophic lateral sclerosis; ALS)は、運動ニューロンの変性・脱落を特徴とする神経変性疾患であり、生涯に約400人に1人の方が発症すると考えられています。ALSは診断から2-5年で死亡にいたることも多い一方で、発症から診断まで平均して1年程度を要するとする研究もあり、早期診断のための検査法の開発が求められています。
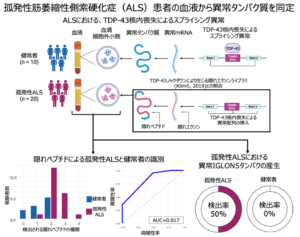
ALSで特徴的な病態として、運動ニューロンの核内のTDP-43が核外に漏出し、蓄積することが知られています。TDP-43は、DNAから転写されるmRNA前駆体に結合してmRNAの完成に必要なスプライシングを補助する役割があります。スプライシングとは、mRNA前駆体から、タンパク質合成に不要な領域(イントロン)を切り取り、必要な領域(エクソン)を繋ぎ合わせて成熟したmRNAを作る核内でのRNA編集プロセスのことです。ALSでは、TDP-43が核内から喪失することでスプライシング制御が破綻し、イントロンの一部の領域が切り取られずに成熟mRNAに残る現象が生じます。これは隠れエクソン(cryptic exon)の挿入と呼ばれています。しかし、隠れエクソンは主に細胞核内で生じるスプライシング異常に起因する現象であり、TDP-43に関連したスプライシング異常を臨床検体から直接検出することは困難です。一方で、mRNAが翻訳されて生じるタンパク質は細胞質に存在し、細胞が放出する血清細胞外小胞を介して血液に運ばれるため、血液検体からその内容を調べることができます。
そこで本研究では、隠れエクソンが翻訳されることでタンパク質中に挿入される異常なアミノ酸配列である「隠れペプチド」を含むタンパク質が、血清細胞外小胞に含まれるという仮説を検証しました。さらに、血清細胞外小胞に含まれる隠れペプチドが、ALSの診断に有用なバイオマーカーとなり得るかを検討するため、健常者とALS患者の識別能を検証しました。
本研究では、ALS患者20名と健常者10名を対象に、血清細胞外小胞のプロテオミクス解析を実施しました。血清細胞外小胞中のタンパク質全体からTDP-43機能異常によって生じる隠れペプチドを絞り込むため、既に報告されている人工多能性幹細胞由来脊髄運動ニューロンにおけるTDP-43発現抑制実験のデータ(Klim et al., 2019)を活用しました。TDP-43の発現減少により生じる隠れエクソンから、候補となる隠れペプチド配列を網羅的に推定し、それぞれの有無を解析しました。その結果、ALS患者の中で4種類の隠れペプチド配列が検出されました。健常者でも検出される隠れペプチド配列もあった一方で、IGLON5タンパク質内に挿入される隠れペプチドはALS患者でのみ検出されました。また、4種類の隠れペプチドの中で検出される種類は、ALS患者で健常者よりも有意に多く、健常者とALS患者を高精度に識別することが可能であることも明らかになりました(曲線下面積 (AUC) = 0.82)。
本研究成果は、ALSにおける血液検査の開発と、疾患メカニズムの理解の進展を通じて、ALSの臨床に資する可能性があります。TDP-43機能異常は運動神経疾患の中ではALSに特異性が高いため、TDP-43機能異常を検出するバイオマーカーの開発は、ALSの診断を補助することが期待されています。本研究はTDP-43機能異常に由来するペプチドを血液中で検出することがALSの診断に有用である可能性を示すものですが、臨床的に応用されるためには、他の運動神経疾患との識別能の検証や、他のバイオマーカーとの組み合わせにおける有用性などを、引き続き研究する必要があります。また、本研究では検出される隠れペプチドの種類を数えましたが、今後はより高感度なプロテオミクスによる隠れペプチドの定量的分析と、機械学習手法などを組み合わせることにより、バイオマーカーとしての臨床応用に向けた改善も期待されます。
また、ALSのメカニズムの理解という点では、隠れペプチドの役割を今後研究することが重要です。隠れエクソンの多くは適切に翻訳されずに分解されることが知られており (Sinha et al., 2025)、TDP-43機能異常によるスプライシング異常については、mRNA分解による遺伝子発現低下の影響に関する研究がこれまで進んでいました(Klim et al., 2019ほか)。本研究は、それに加えて、翻訳を受けて生じる隠れペプチドもALS患者の多くに見られることを示しており、今後はALSのメカニズムの中での隠れペプチドの役割についても研究する必要があります。その一例として、隠れペプチドは免疫細胞にとって非自己と認識され、自己免疫反応を惹起する可能性があること(Chizari et al., 2025)が分かってきています。
以上の内容について、『Inflammation and Regeneration』誌に報告しました(貢献内容:ALSの病態に関連する隠れペプチドの同定)。
Keywords: Biomarker; Cryptic exon; Cryptic peptide; Proteomics; Sporadic amyotrophic lateral sclerosis; TDP-43
Author: Koki Takahashi*, Chris Kato*, Koji Ueda, Shiho Nakamura, Fumiko Ozawa, Nobuko Moritoki, Shinsuke Shibata, Shinichi Takahashi, Satoru Morimoto†, Hideyuki Okano† (*equally contributed, †correspondence)
Inflamm Regen. 2026 Jan 29. doi: 10.1186/s41232-026-00404-w.
投稿者プロフィール

- Project Associate Professor
-
Satoru Morimoto, M.D., Ph.D.
Keio University Regenerative Medicine Research Center (KRM)
Project associate professorResearch Gate Building TONOMACHI 2, 4B, 3-25-10, Tonomachi, Kawasaki-ku, Kawasaki-shi, Kanagawa,
210-0821, Japan
最新の投稿
 ノンドメインブログ2026.03.01第九節 カハールのドグマを塗り替える神経幹細胞治療の司令塔(最終回)
ノンドメインブログ2026.03.01第九節 カハールのドグマを塗り替える神経幹細胞治療の司令塔(最終回) ノンドメインブログ2026.02.16第八節 あらゆる可能性に向けた 再生医療へのどとう怒濤の挑戦
ノンドメインブログ2026.02.16第八節 あらゆる可能性に向けた 再生医療へのどとう怒濤の挑戦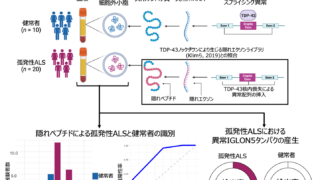 令和7年度(FY2025)2026.01.29Diagnostic potential of cryptic exon-derived peptides in serum extracellular vesicles for sporadic amyotrophic lateral sclerosis
令和7年度(FY2025)2026.01.29Diagnostic potential of cryptic exon-derived peptides in serum extracellular vesicles for sporadic amyotrophic lateral sclerosis ノンドメインブログ2026.01.01第七節 臨床に応用できて価値がある 再生医療への本格的挑戦
ノンドメインブログ2026.01.01第七節 臨床に応用できて価値がある 再生医療への本格的挑戦

